2026年2月12日,国际学术期刊《PLoS Pathogens》-《公共科学图书馆·病原体》在线发表了77779193永利官网海洋学院陈新华团队的最新研究成果,论文题目为“Structural and mechanistic insights into caseinolytic protease inhibition for antimicrobial development against Pseudomonas plecoglossicida” -“基于酪蛋白水解酶结构解析与抑制机制的新见解助力抗变形假单胞菌药物研发”。大黄鱼(Larimichthys crocea, Lc)是我国重要的海水经济鱼类,变形假单胞菌(Pseudomonas plecoglossicida,Pp)是导致其内脏白点病(VWND)的病原,该病每年流行给大黄鱼养殖业造成重大经济损失。该研究揭示了大黄鱼变形假单胞菌中一种具有独特Ser-His-Pro催化三联体的酪氨酸蛋白酶PpClpP1的水解机制,并且蛋白酶抑制剂硼替佐米(Bortezomib,BTZ)可特异性靶向PpClpP1对变形假单胞菌起到抑菌作用。这一发现不仅为理解变形假单胞菌的致病机制提供了新视角,也为有针对性地研发新型水产抗菌药物提供了关键靶点。

Clp(Caseinolytic protease)蛋白酶系统是一种在细菌、古菌以及真核生物的线粒体和叶绿体中广泛存在的ATP依赖性蛋白质降解系统。其在细胞内蛋白质质量控制、错误折叠或受损蛋白的清除以及特定生理过程的调控中扮演着重要角色。研究表明,酪蛋白水解酶(ClpP)是一种新兴的抗菌靶点,但关于水产病原菌ClpP蛋白水解机制的研究却知之甚少。
该研究发现大黄鱼变形假单胞菌中存在两种同源的ClpP蛋白酶亚基—PpClpP1和PpClpP2。生化分析表明,PpClpP2催化效率显著较高;而PpClpP1则相对活性较低(图1)。借助冷冻电镜技术,研究团队成功解析了PpClpP1的三维结构(图2)。结果显示,PpClpP1虽然组装成典型的十四聚体结构,却拥有两个与众不同的特征:一是非常规的“丝氨酸-组氨酸-脯氨酸”催化三联体构型(传统为丝氨酸-组氨酸-天冬氨酸),二是异常扩张的轴向孔道。相比之下,结构模拟预测的PpClpP2则具有与解折叠酶PpClpX相互作用的关键元件,而这些元件在PpClpP1中完全缺失。
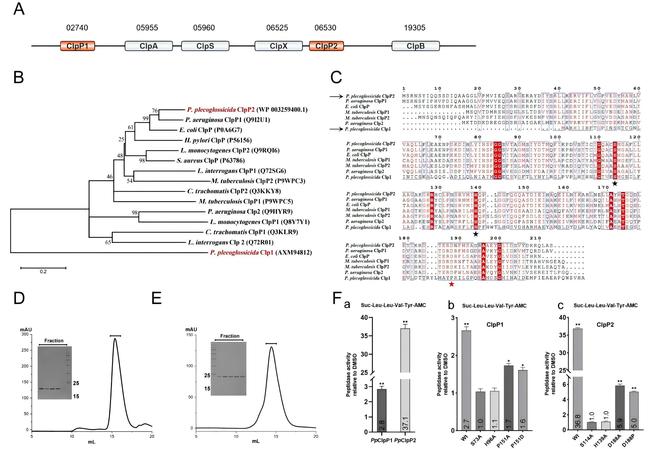
图1. 变形假单胞菌ClpP蛋白酶的鉴定与酶活分析
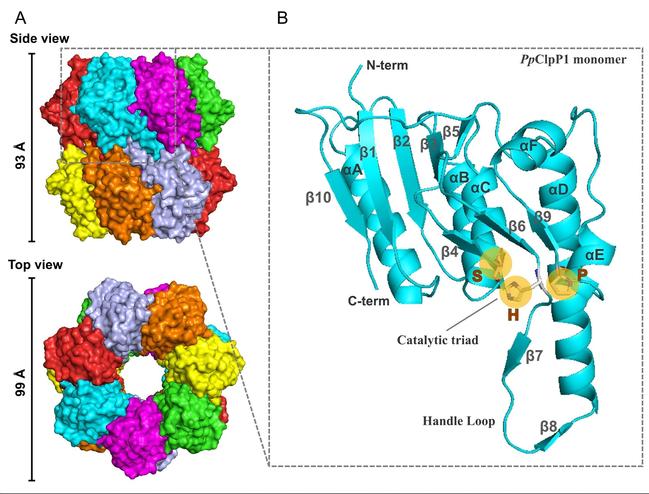
图2. PpClpP1蛋白十四聚体的冷冻电镜结构
进一步研究发现,解折叠酶PpClpX能特异性地识别PpClpP2,无论PpClpP2是单独存在还是与PpClpP1形成异源复合物,均可组装成具有活性的蛋白酶全复合物。特别值得注意的是,PpClpP1P2-ClpX复合物的蛋白水解能力超过了PpClpP2-ClpX复合物,提示异源聚合可能是提升病原菌蛋白酶功能输出的巧妙机制。
蛋白酶抑制剂硼替佐米对变形假单胞菌表现出抑制作用。通过等温滴定量热实验(ITC)和分子对接等前沿技术,证实BTZ能特异性结合PpClpP1(而非PpClpP2),从而抑制其酶活(图3)。基因敲除实验证实,BTZ的抑菌效果正是依赖于靶向PpClpP1实现,敲除该基因后,药物便失去了作用。该研究首次报道了变形假单胞菌PpClpP1蛋白酶的结构特征,揭示了针对该病原菌的ClpP抑制机制,不仅丰富了对病原菌蛋白质降解系统及致病机制的认知,也为有针对性地开发新型水产抗菌药物提供了关键靶点。
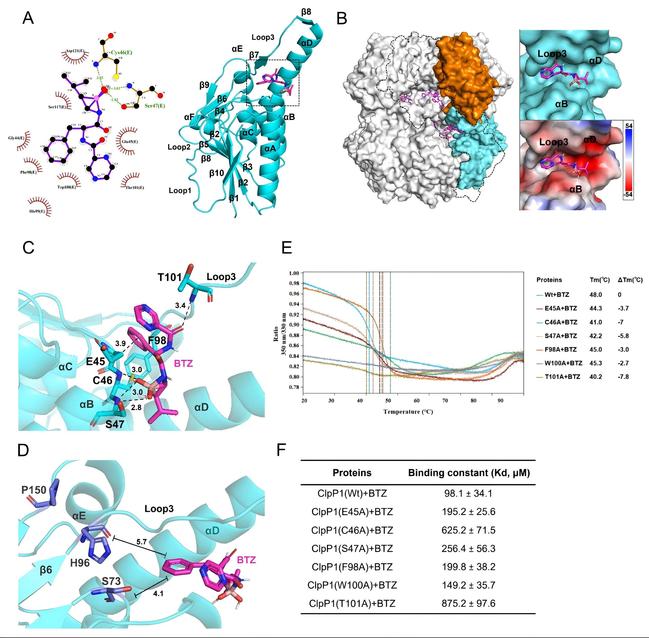
图3. PpClpP1与BTZ结合模式的解析
77779193永利官网海洋学院陈新华教授团队博士研究生陈景杰为论文的第一作者,福建师范大学欧阳松应教授团队,华中农业大学张永安教授团队,以及安徽大学陈学敏教授团队为论文共同合作单位。该研究工作得到了国家重点研发计划、国家自然科学基金、国家现代农业产业技术体系等项目的资助。
论文链接:https://doi.org/10.1371/ journal.ppat.1013909
